Phản ứng thủy phân C4H6O2 trong môi trường axit là một chủ đề quan trọng trong hóa học hữu cơ, đặc biệt là trong chương trình học phổ thông. Bài viết này sẽ giúp bạn hiểu rõ về phản ứng này, từ cơ chế, các yếu tố ảnh hưởng đến ứng dụng thực tiễn. Chúng ta sẽ cùng nhau khám phá thế giới thú vị của hóa học hữu cơ và tìm hiểu tại sao C4H6O2 lại có phản ứng đặc biệt này. thủy phân este c4h6o2 trong môi trường axit
C4H6O2 là gì? Và có bao nhiêu đồng phân este?
C4H6O2 là công thức phân tử của một số hợp chất hữu cơ, trong đó quan trọng nhất là các este. Cụ thể, C4H6O2 có 4 đồng phân este mạch hở, bao gồm: HCOOCH=CH-CH3, HCOOCH2-CH=CH2, CH3COOCH=CH2 và CH2=CHCOOCH3. Mỗi đồng phân này đều có tính chất hóa học riêng biệt, mặc dù có cùng công thức phân tử.
Cơ chế Thủy phân C4H6O2 trong Môi trường Axit
Phản ứng thủy phân C4H6O2 trong môi trường axit là phản ứng thuận nghịch, trong đó este phản ứng với nước tạo thành axit cacboxylic và ancol tương ứng. Axit đóng vai trò chất xúc tác, làm tăng tốc độ phản ứng. Cơ chế phản ứng bao gồm các bước tấn công của nước vào nhóm cacbonyl, proton hóa oxy và cuối cùng là tạo thành sản phẩm.
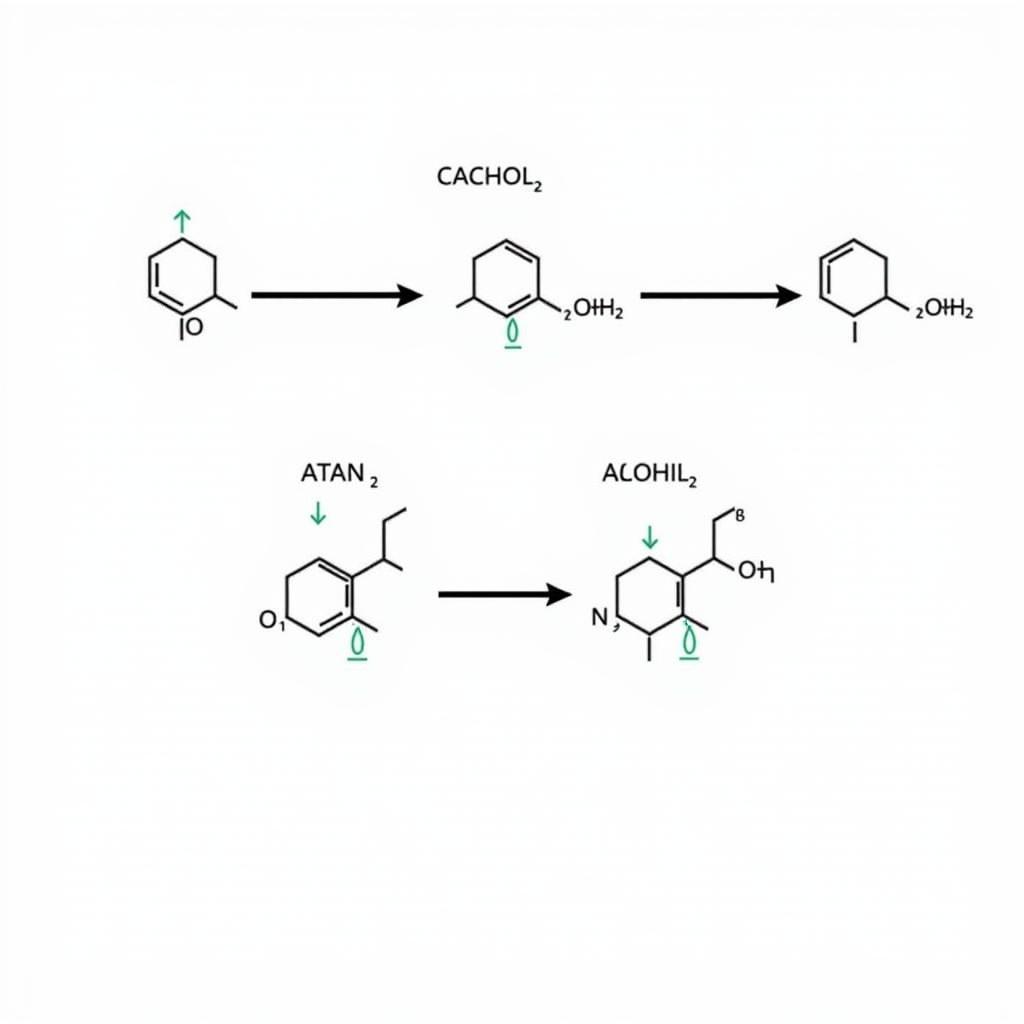 Cơ chế thủy phân C4H6O2 trong môi trường axit
Cơ chế thủy phân C4H6O2 trong môi trường axit
Các Yếu Tố Ảnh Hưởng đến Phản Ứng Thủy Phân
Tốc độ phản ứng thủy phân C4H6O2 bị ảnh hưởng bởi nhiều yếu tố, bao gồm nồng độ axit, nhiệt độ và bản chất của este. Nồng độ axit càng cao, tốc độ phản ứng càng nhanh. Tương tự, nhiệt độ cao cũng làm tăng tốc độ phản ứng. thủy phân este trong môi trường axit Bản chất của gốc axit và gốc ancol trong este cũng ảnh hưởng đáng kể đến tốc độ phản ứng.
Ảnh hưởng của Nồng độ Axit
Nồng độ axit đóng vai trò quan trọng trong việc xúc tác phản ứng thủy phân. Nồng độ axit càng cao, phản ứng diễn ra càng nhanh.
Ảnh hưởng của Nhiệt độ
Nhiệt độ cũng là một yếu tố quan trọng ảnh hưởng đến tốc độ phản ứng. Nhiệt độ cao sẽ làm tăng tốc độ phản ứng.
Ứng Dụng của Phản Ứng Thủy Phân C4H6O2
Phản ứng thủy phân C4H6O2 có nhiều ứng dụng trong thực tế, đặc biệt là trong công nghiệp sản xuất axit cacboxylic và ancol. Ví dụ, thủy phân vinyl axetat (CH3COOCH=CH2) sẽ tạo ra axit axetic và acetaldehyde, là những nguyên liệu quan trọng trong nhiều ngành công nghiệp.
“Việc hiểu rõ cơ chế và các yếu tố ảnh hưởng đến phản ứng thủy phân C4H6O2 là nền tảng quan trọng cho việc ứng dụng phản ứng này trong thực tế,” – PGS.TS. Nguyễn Văn A, chuyên gia hóa học hữu cơ.
Kết luận
Thủy phân C4H6O2 trong môi trường axit là một phản ứng quan trọng trong hóa học hữu cơ, với nhiều ứng dụng thực tiễn. Hiểu rõ cơ chế và các yếu tố ảnh hưởng đến phản ứng này giúp chúng ta kiểm soát và tối ưu hóa quá trình thủy phân, phục vụ cho các mục đích sản xuất và nghiên cứu. C4H6O2 và phản ứng thủy phân của nó là một ví dụ điển hình cho thấy sự đa dạng và phong phú của hóa học hữu cơ. giá tiêu thị trường
FAQ
- C4H6O2 có bao nhiêu đồng phân este?
- Cơ chế thủy phân C4H6O2 trong môi trường axit diễn ra như thế nào?
- Nồng độ axit ảnh hưởng như thế nào đến tốc độ phản ứng thủy phân?
- Nhiệt độ có vai trò gì trong phản ứng thủy phân C4H6O2?
- Ứng dụng của phản ứng thủy phân C4H6O2 trong thực tế là gì?
- Tại sao phản ứng thủy phân C4H6O2 lại quan trọng trong hóa học hữu cơ?
- Có những phương pháp nào để tối ưu hóa quá trình thủy phân C4H6O2?
“Phản ứng thủy phân este, bao gồm cả C4H6O2, là một trong những phản ứng cơ bản và quan trọng nhất trong hóa học hữu cơ, có ứng dụng rộng rãi trong nhiều lĩnh vực,” – TS. Trần Thị B, giảng viên hóa học.
Các tình huống thường gặp câu hỏi
- Học sinh muốn tìm hiểu sâu hơn về phản ứng thủy phân este.
- Giáo viên cần tài liệu tham khảo để giảng dạy.
- Các nhà nghiên cứu muốn tìm hiểu ứng dụng của phản ứng thủy phân C4H6O2.
Gợi ý các câu hỏi khác, bài viết khác có trong web.
- Tìm hiểu về các loại este khác.
- Xem thêm về phản ứng xà phòng hóa. trường trung học cơ sở quận tân phú